 |
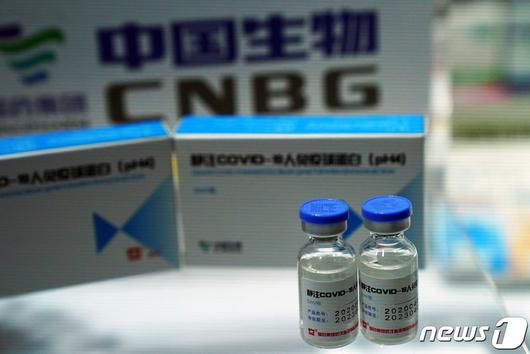
중국 국영 제약사 시노팜 자회사 CNBG가 개발한 코로나19 백신 © 로이터=뉴스1 |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
(서울=뉴스1) 박혜연 기자 = 중국 국영제약사 시노팜이 자회사 중국국립생명공학그룹(CNBG)이 개발한 신종 코로나바이러스 감염증(코로나19) 백신을 공식 승인해달라고 중국 규제당국에 신청서를 제출했다.
25일 블룸버그통신 등에 따르면 스성이 시노팜 부사장은 중동과 남미에서 실시한 임상 3상 중간 분석 결과와 함께 중국 국가의약국에 승인 신청서를 제출했다고 밝혔다.
CNBG 백신이 공식 승인되면 중국은 러시아에 이어 세계 두 번째로 당국의 승인을 얻어 백신을 일반에 공급할 수 있게 된다.
시노팜 홍콩법인 등 관련주는 이 소식이 전해진 후 급등했다.
앞서 류진전 시노팜 회장은 지난달 CNBG의 백신이 아랍에미리트와 요르단, 아르헨티나, 이집트, 페루, 브라질 등 10개국에서 6만명을 대상으로 임상 3상을 진행 중이라고 밝혔다.
CNBG 백신은 지난 7월 중국 당국의 긴급사용 승인을 받아 중국에서 지금까지 100만명에 달하는 사람들에게 접종됐다. 류 회장은 "삼각한 부작용은 단 한 건도 보고되지 않았다"고 주장했다.
CNBG 백신은 비활성화돼 인간 세포에서 복제가 불가능한 바이러스를 이용해 개발된 것으로 알려졌다. 미국 제약사 모더나·화이자가 개발한 백신처럼 2회 접종이 필요하다.
류 회장은 "우리 백신을 맞고 해외로 나간 건설회사 직원이나 외교관, 학생 중에 감염자는 한 명도 나오지 않았다"고 강조했다.
하지만 CNBG의 백신 임상시험 결과는 지금까지 공개된 적이 없어 안전성 논란은 이어질 것으로 보인다. 전문가들은 표준 임상시험에 따른 통제된 그룹에서 비교 가능한 결과가 나오지 않는 이상 긴급사용 승인 후 자료만 갖고 효능을 판단하는 것은 이르다고 입을 모은다.
hypark@news1.kr
[© 뉴스1코리아(news1.kr), 무단 전재 및 재배포 금지]
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


